- トップ
- > 研究者・企業の方へ
- > 研究所について
- > 各研究部門の紹介
- > 分子内分泌研究部
- > オリジナルサイト
- > シルバー・ラッセル症候群 (Silver-Russell症候群 SRS: OMIM 180860)
シルバー・ラッセル症候群 (Silver-Russell症候群 SRS: OMIM 180860)
疾患概要
Silver-Russel 症候群 (SRS) はSGA性低身長を示す代表的なインプリンティング疾患で、臨床像に基づいて診断されます。 国際的合意を得たSRSの臨床診断基準は6つの項目(SGA出生、低身長、相対的大頭、前額突出、哺乳不良、体の左右非対称)のうち4項目をみたせばSRSと診断します。
SGA性低身長:在胎週数に比較して小さく生まれ(SGA出生)、その後も身長がキャッチアップせず低身長を示す
発症頻度
SRSの頻度は16,000出生に1人と報告されています(Eggermann T et al. 2023)。
臨床像
国際的コンソーシアムによりNetchine-Harbison clinical scoring system (NH-CSS)をSRSの臨床診断基準として用いることが提唱されています。NH-CSSは下記の通りです。NH-CSS 4点以上でSRSと診断されます。3点であっても、SRSを疑わせる臨床所見(第5指の屈曲、逆三角形の顔貌など)を認める場合は、SRSの遺伝子診断が推奨されます。遺伝型と表現型の関係については、H19/IGF2:IG-DMR (H19-DMR) 低メチル化は他の原因に比べて出生体重が小さいこと、出生時の頭囲が比較的保たれており、相対的大頭を示す割合が多いこと、体の左右非対称を多く示すことが報告されています。一方、7番染色体母性片親性ダイソミー (UPD(7)mat) は、精神・運動発達遅延や言葉の遅れを示す割合が他の原因に比較して多いとの報告があります。
SRSで認める出生後の成長障害は、食欲不振や口腔内違和感による摂食障害 による栄養摂取量の不足が大きな原因と考えられます。栄養摂取不足や筋肉量が少ないことからストレスがかかる状況(発熱、手術など)では低血糖のリスクがあります。体の発育に関しては、未治療の場合、最終身長は、-3 SD程度との報告があり、早期から成長ホルモン治療が推奨されます。また、思春期開始時期は正常範囲内であるものの早めとの報告があります。早く思春期が来てしまうと早く身長が止まってしまいます。定期的に小児内分泌科でフォローを受ける必要があります。その他、顎が小さいことにより歯並びが悪くなることもあり、保険適応で歯科矯正を受けられます。
|
Netchine-Habison clinical scoring system(SRSの臨床診断基準) |
|
|
①SGA出生 |
|
|
出生体重 and/or 出生身長が-2 SD以下 |
|
|
②出生後の成長障害(低身長) |
|
|
24±1 カ月の身長が-2 SD以下もしくは身長がtarget heightの -2 SD以下 |
|
|
③相対的大頭 |
|
|
出生時の頭位SDが出生体重 and/or 出生身長SDより1.5 SD 以上大きい |
|
|
④前額突出(1~3歳で評価) |
|
|
⑤体の左右非対称 |
|
|
脚長差0.5cm以上もしくは腕の長さの差もしくは脚長差が0.5cm以内でも顔以外の体の2以上のパーツで非対称がある |
|
|
⑥哺乳不良、低BMI (≤-2 SD) |
|
|
24か月時にBMIが -2 SD以下もしくは経管栄養の必要もしくは食欲亢進のためにcyproheptadine (商品名ペリアクチン)の使用 |
|
図1. 遺伝学的原因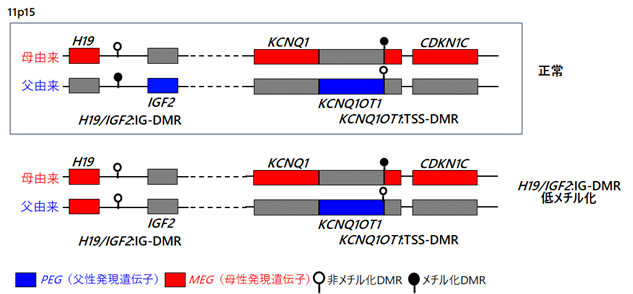
SRSは父性発現遺伝子IGF2の発現低下による病態(図1)と、7番染色体がともに母に由来するUPD(7)mat が主たる原因となります。臨床診断基準が非特異的なこともあり、臨床診断基準を満たしている症例のなかには、同じインプリンティング疾患であるTemple症候群や、染色体異常が含まれことがあります。図2は、我々が遺伝子解析を行ったSRSの臨床診断基準を満たした178名の解析結果を示しています。H19-DMRの低メチル化を約30%に、UPD(7)matを約5%に認めました。SRSの原因として判明している原因が同定されたのは38.2%でした。その他、Temple症候群をはじめとした様々なインプリンティング疾患が約10%に同定されましたが、約半数では原因不明でした。
図2. SRS臨床診断基準をみたした症例における遺伝学的原因別頻度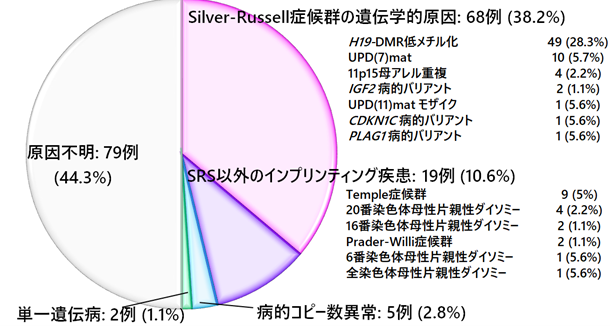
遺伝診断法および遺伝学的診断機基準
SRSの主要な原因であるH19-DMRの低メチル化やUPD(7)matの同定には、メチル化解析が推奨されます。DMRのメチル化状態とコピー数変化を同時に解析することのできる、メチル化特異的MLPA法(MS-MLPA)が有用です。MS-MLPAは、成育医療研究センター衛生検査センター(非保険)と当研究室(研究の一環)で行っております。SRSの場合、Temple症候群や、20番染色体母性片親性ダイソミー、6番染色体母性片親性ダイソミーを持つ患者でもSRS表現型を示すことが判明しているので、すべてのインプリンティング疾患をスクリーニングできるME034のキットを用いたMS-MLPA法による解析が推奨されます。メチル化異常を認めなかった症例については、病的バリアントがSRS表現型を来すことが判明しているIGF2、CDKN1C、PLAG1、HMGA2遺伝子の変異検索を行うことになります。かずさDNA研究所での遺伝学的検査のインプリンティング疾患解析パネル(非保険)に、これらの遺伝子は含まれています。
管理・治療法
新生児期、乳児期は栄養状態の改善、身長のキャッチアップを目指します。SGA出生児において、急速に栄養状態が改善することは、将来のメタボリック症候群のリスクとなるとの報告がありますので、注意が必要です。食事摂取に影響する口部運動や口内感覚に関する問題についての評価や、ある場合は治療をすることも必要となります。乳幼児期は、低血糖のリスクがあり、特に体調不良時など体にストレスがかかる状況では血糖測定が推奨されます。また、手術時には、ケトン尿、低血糖を避けるために、手術前日夜からのブドウ糖輸液を開始し、術後は経口摂取が可能となっていから退院する必要があります。SGA性低身長としてGH治療は行われており、SRS患者へのGH治療の有用性は立証されていますので、早期からのGH治療の開始が推奨されます。SRS患者の骨年齢は、はじめは遅れているが、8~9歳ごろに急激に進むと報告されています。思春期の開始は正常範囲ですが、早い傾向にあり、思春期の早い発来により最終身長が小さくなってしまいます。定期的に小児内分泌科を受診し、低身長での思春期早発傾向がある場合はGnRH アナログ製剤治療も考慮する必要があります。SGA出生児はメタボリック症候群のリスクがあると報告されています。特にGH治療終了後は、極端な体重増加をさけ、健康的な食事 (特に適切なタンパク摂取)やライフスタイル(特に運動)を心掛け、メタボリック症候群の有無の確認のためにも定期的な受診をお勧めします。精神運動発達の遅れや言葉の遅れを認めるSRS患者さんもいます。早期の発達評価と必要な場合のリハビリ、療育の開始することを推奨します。
予後
予後は良好ですが、成人になってからの糖尿病や脂質代謝異常の合併などのリスクが報告されていますが、大規模な研究はまだありません。定期的な血液検査などは、GH治療が終了してからも行ったほうがいいでしょう。
小児、指定難病ページ、各大学、関連学会へのリンク
患者会



