炎症性腸疾患(IBD)の発症に関与する新たな遺伝子変異を初めて同定~生物学的製剤による治療に成功した小児症例の報告~
この成果は、科学雑誌『Intestinal Research』に2025 年4 月4 日付で掲載されました。
[1]TRAF3 とは、TNF 受容体関連因子 (TRAF)に属する分子の一つで、生体シグナルを制御して、過剰な炎症を抑制するタンパク質のこと。
[2]炎症性腸疾患とは、消化管に慢性的な炎症を引き起こす原因不明の疾患で、主にクローン病と潰瘍性大腸炎が含まれます。
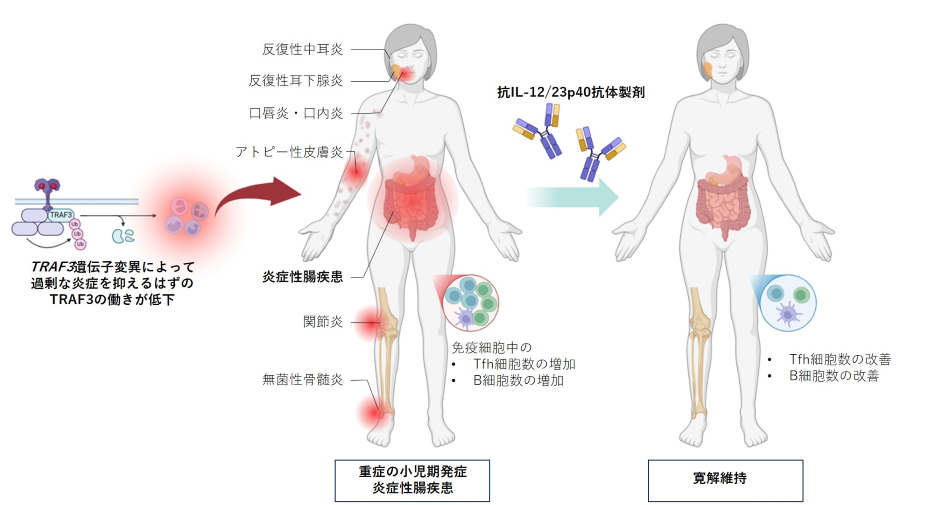 【図1】今回報告された小児期発症炎症性腸疾患のイメージ
【図1】今回報告された小児期発症炎症性腸疾患のイメージプレスリリースのポイント
- 反復性耳下腺炎など、腸炎以外の症状も伴っていた小児期発症IBDにおいて、TRAF3遺伝子に新たな変異を同定し、この変異がIBDの発症に関与する可能性を示しました。
- TRAF3遺伝子変異が関与していた本患者さんのIBD は非常に重症であり、通常のIBD治療で使われるチオプリン製剤および抗TNFα抗体製剤では治療が困難でしたが、Tフォリキュラー (Tfh)[3]細胞に作用する抗インターロイキン[4](IL)-12/23p40抗体製剤の導入により長期的な臨床的寛解が得られました。
- TRAF3変異がある患者さんでは腸炎の活動期に末梢血中の免疫グロブリン[5]の値が異常に高く、免疫細胞を調べると免疫グロブリン産生に関与するB細胞とTfh細胞の増加が認められましたが、治療によって寛解するとこれらの異常が改善することが示されました。
[4]インターロイキンとは、細胞間の連携に使用される物質のグループで、免疫応答や炎症反応の調節において重要な役割を果たします。
[5]免疫グロブリンとは、抗体ともいわれる血液中のタンパク質の一種で、病原体から体を守る役割がありますが、異常に活性化すると病気の原因となることがあります。
研究の背景
IBDは消化管の慢性的な炎症を特徴とする疾患であり、主にクローン病と潰瘍性大腸炎に分類されます。IBD患者さんの2~3割が小児期に発症し、小児患者さんの数は日本を含めて世界的に増加しています。原因不明の疾患であり、一般的に環境要因と遺伝要因が複雑に合わさって発症すると言われている一方で、近年の遺伝学的研究により、若年発症のIBD患者さんの中には単一遺伝子の変異によって免疫に異常が生じることで発症するIBDが複数報告されており、当センターではその病態解明に注力しています。
TRAF3は体内に生じた過剰な炎症を制御する機能があり、2022年に初めて、自己免疫疾患や免疫不全を引き起こす遺伝性疾患の原因としてTRAF3遺伝子が報告されていましたが、IBD との関連はこれまで明らかになっていませんでした。
研究内容・成果の要点
これまでTRAF3変異の症状として報告されている反復性中耳炎、耳下腺炎やアトピー性皮膚炎に加えて、重度の口唇炎・口内炎、さらには無菌性骨髄炎を伴う1 名の小児IBD 患者さんにおいて、全エクソーム解析[6]を実施し、新たにTRAF3の遺伝子変異(p.Pro487Leufs*8)を同定しました。この変異により、TRAF3タンパク質の発現が低下し、末梢血中Tfh 細胞の増加を伴う異常な免疫活性が確認されました。
この患者さんではIBD に対する初期治療として使用されたチオプリン製剤および抗TNFα抗体製剤の効果が乏しく、再燃が繰り返されました。しかし、Tfh細胞に作用する抗IL-12/23p40 抗体による治療により、IBDの持続的な臨床的寛解が得られ、末梢血中のTfh 細胞数を含む免疫異常が正常化されました。
[6]全エクソーム解析とは、遺伝子の中でタンパクになる情報がコードされた配列のみを網羅的に解析する遺伝子解析の手法です。
発表論文情報
論文タイトル:Inflammatory bowel disease in a young female patient with a novel de novo TRAF3 frameshift variant responsive to ustekinumab(ウステキヌマブに反応した新規 de novo TRAF3フレームシフト変異を有する若年発症IBD)
掲載誌:Intestinal Research(2025年4月4日付)
著者:竹内 一朗1, 谷口 公介2,3, 新井 勝大1, 内山 徹4, 寺尾 美穂5, 堀 あすか2, 河合 利尚6, 義岡 孝子7, 京戸 玲子1, 清水 泰岳1, 藤多 慧8,9, 本村 健一郎8, 岡崎 有香2, 石川 尊士6, 小椋 雅夫10, 林 健太郎11, 松本 健治8, 高田 修治5, 小野寺 雅史6, 森田 英明8,12, 秦 健一郎2,3
所属:
1. 国立成育医療研究センター 小児炎症性腸疾患センター・消化器科
2. 国立成育医療研究センター 周産期病態研究部
3. 群馬大学大学院医学系研究科 分子細胞生物学
4. 国立成育医療研究センター 成育遺伝研究部
5. 国立成育医療研究センター システム発生・再生医学研究部
6. 国立成育医療研究センター 免疫科
7. 国立成育医療研究センター 病理診断部
8. 国立成育医療研究センター 免疫アレルギー・感染研究部
9. 東京慈恵会医科大学 小児科
10. 国立成育医療研究センター 腎臓・リウマチ・膠原病科
11. 国立成育医療研究センター 整形外科
12. 国立成育医療研究センター アレルギーセンター
DOI:10.5217/ir.2024.00190
- 本件に関する取材連絡先
-
国立成育医療研究センター 企画戦略局 広報企画室
03-3416-0181(代表)
koho@ncchd.go.jp
月~金曜日(祝祭日を除く)9時〜17時
※医療関係者・報道関係者以外のお問い合わせは、受け付けておりません。



